IL SOTTOSCRITTO NON POSSIEDE ALCUN DIRITTO SUL TESTO DELL’ESERCIZIO.
ESERCIZIO
La polimerizzazione in massa dello stirene avviene in
presenza del solo monomero, di un opportuno iniziatore e di agenti di trasferimento
di catena. Una corrente di 7000 kg/h a 25°C la cui composizione è nota viene alimentata a due reattori perfettamente miscelati in serie, seguiti
da un reattore a pistone. L’esigenza di avere tre diversi reattori è legata
alla crescita di viscosità del sistema, il che richiede differenti sistemi di
movimentazione o miscelazione.
Il flowsheet del sistema è il seguente:
Dati su FEED:
Composizione della corrente alimentata
Pressione
|
1
|
atm
|
Temperatura
|
25
|
°C
|
Portata
|
7000
|
kg/hr
|
Componente
|
Descrizione
|
Fraz. massica
|
Di-t-butilperossido (TBP)
|
iniziatore
|
0.0003
|
Stirene (STY)
|
monomero
|
0.98
|
Etilbenzene (EB)
|
agente di trasf. catena
|
0.019
|
N-dodecil mercaptano (DDM)
|
agente di trasf. catena
|
0.0007
|
Dati dei reattori e condizioni operative:
“La polimerizzazione avviene in fase liquida nei tre reattori. Il primo CSTR opera ad una temperatura di 120°C, il secondo a 160 °C ed entrambi hanno un volume di 20 m3. Il terzo reattore opera in un intervallo termico che varia fra 160-200°C fra ingresso ed uscita, ha un diametro di 0.4 m ed è lungo 80 m. Tutto il sistema opera alla pressione atmosferica.”
I DATI CINETICI VERRANNO PRESENTATI IN SEGUITO.
SIMULAZIONE:
- simulare il
processo e diagrammare gli andamenti delle curva di
distribuzione ponderali del peso molecolare all’uscita dei tre reattori;
- diagrammare
l’andamento della conversione, del peso molecolare medio numerico, del peso
molecolare medio ponderale e dell’indice di polidispersità all’uscita di
ciascun reattore in funzione della portata alimentata al processo (FEED) nel
range 4000-9000 kg/h;
- diagrammare
l’andamento della conversione, del peso molecolare medio numerico, del peso
molecolare medio ponderale e dell’indice di polidispersità del prodotto finale
al variare della temperatura di uscita del terzo reattore da 160 a 240 °C;
- diagrammare
l’andamento della conversione, del peso molecolare medio numerico, del peso
molecolare medio ponderale e dell’indice di polidispersità all’uscita di
ciascun reattore in funzione del contenuto di iniziatore (TBP)
nell’alimentazione (FEED). Si faccia variare la frazione massica di TBP nel
range 0.0003-0.003.
INTRODUZIONE
In questa esercitazione si simulerà la polimerizzazione dello stirene a
formare polistirene.
Il polistirene, scoperto per caso da uno speziale che credeva fosse un
semplice prodotto di ossidazione, trova applicazioni in molti campi:
dall’elettronica alla fonderia, dall’isolamento all’imballaggio soprattutto
nella sua forma espansa.
Il gruppo stirenico nella macromolecola ha un ingombro sterico rilevante,
cosa che limita la sistemazione ordinata delle molecole; ciò porta ad una
struttura amorfa del polimero, il quale si presenta trasparente nella sua forma
base.
Nel nostro caso tratteremo la polimerizzazione in massa dove è lo stesso stirene
a fare da solvente.
Il tempo gioca un ruolo fondamentale in questo tipo di processo e
prescindere da questo significherebbe non parlare di realtà ma di fantasia.
L’alimentazione di stirene presenta anche iniziatori ed agenti di
trasferimento di catena.
L’iniziatore termico, TBP nel nostro caso, ha il compito di rendere
sostenuta la formazione di radicali che attaccano il doppio legame del
sostituente vinilico nello stirene, generando delle reazioni a catena di
formazione di radicali con catena sempre più lunga via via che gli attacchi si
susseguono per la stessa catena iniziale.
 |
| Iniziatore termico: perossido che per scissione
omolitica del legame O-O forma due radicali. |
Gli agenti di trasferimento di catena hanno un compito regolatore (del MW)
e non inibitore; ciò significa che la velocità di propagazione del radicale
prodotto dal trasferimento è sostenuta e non costituisce un fattore limitante
per la polimerizzazione. In realtà è vero che si tratta di un AGENTE DI
TRASFERIMENTO ma nel nostro caso gli agenti sono molto poco attivi rispetto
alla propagazione ed hanno una influenza quasi nulla, ergo NON SONO EFFICACI
(bassi coefficienti di trasferimento); lanciando la simulazione senza questi
non si ha alcun cambiamento, in pratica, in alcuna condizione imposta. Il
controllo, in generale, viene effettuato sulla propagazione della catena
facendo in modo che a determinate concentrazioni rilevanti di radicali polimerici, in
funzione di quanto agente si inserisce, abbiano luogo in maniera sostenuta le
reazioni di trasferimento che bloccano la crescita del polimero dando luogo ad
un nuovo radicale di partenza.
L’utilizzo degli agenti di trasferimento assieme ad un corretto dosaggio
dell’iniziatore limitano il cosiddetto effetto gel che rappresenta un
rallentamento della terminazione delle catene causato da una limitante capacità
diffusiva delle macromolecole in un mezzo molto viscoso, divenuto tale per una
crescita non controllata (e non limitata) delle catene polimeriche; NON È IL
NOSTRO CASO.
L’unica reazione di trasferimento significativa risulta quella con il
monomero.
Le reazioni che intervengono nel nostro caso sono molte e quelle
significative sono rappresentate di seguito*:
- decomposizione termica dell’iniziatore
decomposizione termica del monomero
inizio
propagazione
trasferimento col monomero
trasferimento con EB
trasferimento con DDM
terminazione per accoppiamento
*Ci si riferirà spesso a tale schema con la simbologia: numero).
Ad ognuna di queste reazioni sarà associata una cinetica diretta; quelle
inverse sono ritenute trascurabili alle nostre condizioni operative.
Si noti che l’iniziatore viene attivato termicamente e che lo stesso
stirene può dare origine alla formazione di radicali. Oltre alle fasi
precedentemente descritte, quali la formazione del radicale e propagazione
della catena, sono schematizzate le reazioni di trasferimento e terminazione
per accoppiamento (è ritenuto trascurabile il disproporzionamento).
Le cinetiche* afferenti alle precedenti reazioni sono le seguenti:

*Nota: nelle cinetiche NON figurano le concentrazioni di polimero ma di RADICALI POLIMERICI.
La prima costante di radicalizzazione è più alta della seconda che però sarà
rilevante quando le concentrazioni di stirene sono alte.
Si noti il fattore f che tiene conto dell’efficacia di inizializzazione: i
radicali sono specie altamente reattive che facilmente danno luogo a reazioni
parallele quali, per esempio, lo stesso accoppiamento tra i radicali appena
formatisi; non tutti i radicali che si formano dal TBP danno effettivamente
inizio ad una catena polimerica.
Inizio 3) e propagazioni n-esime sono ipotizzati avere medesima cinetica
ciò si basa sul considerare uguale reattività con il monomero indipendentemente
da quante unità monomeriche contiene la catena in propagazione ( 3) è un caso limite); nella realtà qualche
variazione è osservabile fino ad una lunghezza della decina di unità, ma
siccome per il singolo radicale un migliaio di monomeri in media si attaccherà,
ciò è trascurabile.
CENNI E DATI UTILI
Le costanti cinetiche vengono espresse nella formulazione di Arrhenius:
Come è ben noto l’energia di attivazione è sempre positiva per ogni
reazione elementare e k aumenta all’aumentare della temperatura.
Più alta è l’energia di attivazione maggiore sarà la variazione di k con la
T e più bassa tenderà ad essere la kcinetica:
Cosa opposta avviene con il fattore pre-esponenziale, il quale amplifica di
un fattore costante curva e crescita:
Valori di k delle reazioni a diverse temperature:
NOTE
I reattori CSTR hanno un volume uguale (con diversi sistemi di
agitazione magari) mentre il PFR ne ha uno che è circa dimezzato; il PFR consente
un controllo più preciso della temperatura (si ricordi l’aumento della
viscosità che limita il trasporto di calore) e un tempo di residenza medio più
definito, ergo migliore omogeneità dei risultati nella realtà dei fatti. Il
miglior controllo sulla temperatura evita il running away della reazione dovuto
alle reazioni (in pratica alla propagazione) che sono fortemente esotermiche e
che però portano ad incremento di viscosità del fluido inibendo la dissipazione
del calore; ne risulta un aumento di temperatura che favorisce le cinetiche e lo
sviluppo di calore, il tutto in modo ovviamente disomogeneo. Il rapporto
lunghezza/diametro per il PFR è inoltre molto alto cosa che consente di
trascurare gli effetti di bordo di imbocco e sbocco del reattore.
Lo schema cinetico presentato viene affiancato ad una ipotesi molto
importante: stazionarietà (o quasi-) del sistema radicalico; ciò implica che
dopo una prima fase breve di transitorio in cui i radicali vengono formati
molto di più di quanti se ne accoppino, il sistema raggiunga una condizione per
cui i radicali che si formano (per le reazioni di inizio) sono uguali a
quelli che subiscono terminazione, cioè la concentrazione molare dei radicali
non varia con il tempo.
È possibile notare che la reazione 1) e 2) presentano energia di attivazione maggiore della reazione 8) e per questo all'aumentare della temperatura ci si aspetta che aumenti la concentrazione di radicali, che vi siano più inizi e terminazioni: questo tenendo conto solo delle costanti.
Dal punto di vista cinetico è facilmente intuibile che laddove inizialmente
si ha un mare di monomeri l’urto efficace con i
monomeri è molto probabile e le reazioni preponderanti saranno quelle di propagazione(lo saranno sempre dal punto di vista cinetico finché
il monomero non va ad esaurirsi) e trasferimento con monomero; laddove invece la concentrazione di monomero
decresce e quella di polimero cresce le catene hanno maggiori probabilità di
incontrare gli agenti di trasferimento; in
realtà è il trasferimento con monomero che conta maggiormente.
Il metodo termodinamico utilizzato per la valutazione delle proprietà di
miscela è POLYNRTL.
Dal punto di vista delle proprietà fisiche l’iniziatore e gli agenti di
trasferimento non influenzano come tali, perché presenti in piccole quantità,
ma per la loro funzione (almeno l’iniziatore); quindi non si ritiene
fondamentale la presenza nel metodo dei parametri di interazione “non ideale”
tra questi componenti.
RISULTATI ED ANALISI
Una volta inseriti gli schemi di reazione e i dati si lancia la
simulazione.
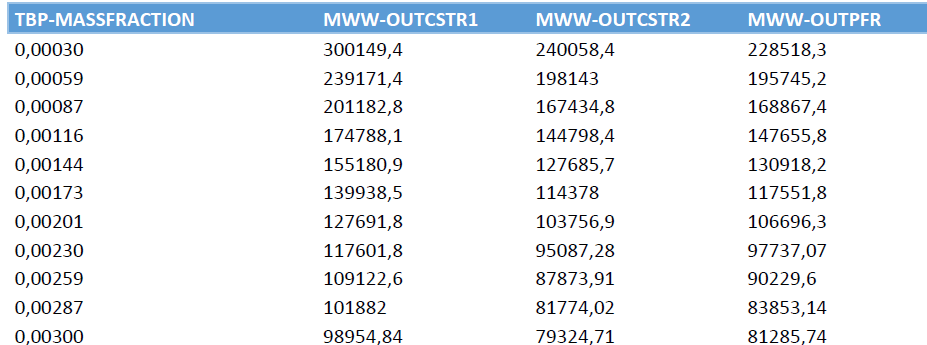
Il polimero nelle tre correnti OUT dai reattori presenta tali distribuzioni
di MW vs frazione in peso delle catene:
È possibile notare come all’uscita del primo reattore si abbia il picco di
frazione in peso a valori maggiori di MW rispetto al polimero uscente dagli
stadi reattivi successivi. È facile intuire che lo stesso ci si aspetta per il
peso molecolare medio.
Ciò può essere spiegato. La conversione in CSTR1 si aggira intorno al 27%,
ciò significa che in questo reattore si è lavorato in abbondanza del monomero (alla
concentrazione in uscita); dunque se ne deduce che hanno avuto maggiore
prevalenza rispetto ai casi successivi le reazioni di propagazione, aumentando
la lunghezza media delle catene (se si lavora a parità di altre condizioni) e meno quelle di inizio/accoppiamento per la temperatura inferiore. Le
reazioni di terminazione/inizio e trasferimento hanno importanza maggiore nei
successivi reattori, dove la concentrazione in radicali e la temperatura ne
aumenteranno le velocità di reazione.
A questo punto se si formano molte molecole che si propagano minormente
influenzate da altre reazioni (almeno rispetto a come lo saranno in seguito) si
avrà un picco di frazione verso MW maggiori dei casi successivi. In effetti il
grado di polimerizzazione medio (rappresentante del numero di unità strutturali
presenti in media nel polimero) è inversamente proporzionale alla velocità di
polimerizzazione la quale aumenta con l’aumentare della temperatura; è anche
vero che la concentrazione dell’iniziatore diminuisce da CSTR1 a CSTR2 e lungo
PFR, la qual cosa, da sola, porterebbe ad una diminuzione della velocità di polimerizzazione
ma la dipendenza dalla concentrazione di in. è minore e prevale l’effetto descritto
in precedenza.
Si noti come l’aumento di temperatura sia benefico per la cinetica del
sistema ed in effetti la conversione dello stirene passa da 27% in CSTR1 a
65%(rispetto a FEED) in CSTR2, nonostante vi sia meno stirene (frazione
inferiore) si ottiene di più (se si considera lo stirene in ingresso al
reattore CSTR2 cioè il 73% del feed e quello in uscita cioè il 35% del feed, si
ha una conversione di (0.73-0.35)/0.73=0.52=52%).
Nel terzo reattore invece è
l’effetto di abbassamento di concentrazione(quantità) del reagente che prevale
rispetto all’aumento di temperatura, in effetti la conversione rispetto al feed
è di 0.83; in realtà, rispetto alla corrente in ingresso al PFR, allo stesso
modo precedente, si ha però una conversione dello stirene del 51%, quindi
intrinsecamente quanto detto in precedenza non è del tutto vero ma è
conseguenza del fatto che viene alimentato meno stirene al PFR.
Si noti che l’energia di attivazione della reazione 4) è minore di quella
della reazione 5) e la 5) subisce un aumento maggiore della costante cinetica
nei due reattori, la restante espressione è identica; una diminuzione del peso
molecolare medio è già solo per questo intuibile.
In effetti valutando il rapporto k4/k5 si può notare
come subisca una diminuzione sensibile nei tre reattori nel primo vale ≈4156
nel secondo ≈2141 e nel terzo, in media, ≈1688; in generale ciò comporta una
diversità delle catene che si formano, al diminuire di questo rapporto ci si
aspettano catene più piccole, trascurando altri effetti.
Intuitivamente se la velocità di propagazione raddoppiasse da valori grandi
e quelle di trasferimento raddoppiassero da valori piccoli, non si avrebbe un
effetto pesante sulle dimensioni delle catene, se non per altri fenomeni e
reazioni; non è il nostro caso dove la prima subisce più di un raddoppio e “quella”
di trasferimento quasi quadruplica. A ciò si uniscono altre reazioni quali l’accoppiamento,
cineticamente molto favorito, che “non fa distinzione tra chi accoppiare”, cioè
può accoppiare radicali lunghi o radicali corti, il risultato dipende dalla
statistica e quindi dalle concentrazioni di tali radicali.
Se si varia la portata di feed ci si aspetta, obbligatoriamente, una
variazione del tempo di permanenza nei reattori, a parità di geometria; se si
riduce la portata, il tempo di permanenza aumenta e con esso la conversione
visto che si prosegue per un tempo più lungo il contatto tra reagenti nel
reattore e quindi si dà un maggiore sviluppo temporale alle cinetiche.
Viceversa laddove tale portata aumenti.
Quanto detto è visibile nel seguente grafico.
Cosa succede al MW medio?
Ovviamente siccome il primo CSTR è quello che lavora in “mare” di monomero,
ci si aspetta che all’aumentare della portata, cioè al diminuire del tempo di
permanenza le catene abbiano meno tempo per crescere e risultino più corte; ma
attenzione anche la formazione di radicali ha meno tempo (se ne formano di
meno) e quindi l’effetto precedente risulta smorzato rispetto a ciò che succede
a valle. Negli altri due reattori le cinetiche sono favorite dalla temperatura e
sono presenti, per questo, monomeri più reattivi dal punto di vista
dell’inizio e trasferimento; inoltre sono più sostenute le reazioni di
trasferimento e terminazione, quindi si ha una caduta del peso
molecolare medio. L’andamento con la portata in alimentazione al processo è
simile alla precedente.
Si consideri ciò che varia con la portata. Se aumenta la portata la
conversione nei reattori diminuisce; se diminuisce la conversione nel primo
reattore significa che al secondo arriva più monomero e TBP e così via per il
terzo.
Se arriva più monomero ai reattori significa che le reazioni N° 2-3-4-5
sono favorite; di queste la 2 ha una cinetica del terzo ordine, mentre le altre
hanno ordine parziale di reazione rispetto allo stirene 1. Le temperature sono
quelle del caso precedente ed incidono nel modo esposto in precedenza. Si
concluda che le variazioni sono dovute essenzialmente per una maggiore
influenza dell’inizio (anche TBP), trasferimenti e terminazioni (T,
quasi-steady state). Si tenga anche conto che anche se la propagazione ha una
velocità di reazione molto più alta di queste non significa che terminazione,
inizio e trasferimento e loro variazioni non influiscano; se fosse
l’opposto non si avrebbe polimerizzazione essenzialmente; la velocità di propagazione
deve essere molto più elevata al fine di formare statisticamente un polimero
prima di terminare la catena.
Si deve anche dire che laddove le cinetiche continuano ad essere sostenute,
arrivano quantità inferiori di polimero (ad alto peso molecolare medio) a CSTR2
e PFR e quindi le reazioni analizzate prima che prendono luogo nei successivi due reattori avranno una influenza ancora
maggiore su ciò che si formerà (si forma essenzialmente in CSTR2 e PFR…).
SI TENGA CONTO CHE IN TUTTA LA RELAZIONE AD ALTO E
BASSO DEVE ESSERE ASSEGNATO UN SIGNIFICATO RELATIVO A CONDIZIONI PRECEDENTI O
DETTE IN PRECEDENZA.
1. Quanto detto si riassume in:
- si formano più radicali nei reattori successivi;
- sviluppo di dimensione delle catene inferiore per lo sviluppo dei radicali nelle condizioni di CSTR2 e PFR;
- sviluppo numerico di catene inferiore nel primo reattoreà maggiore influenza reazioni in CSTR2 e PFR;
- trasferimento più significativo;
- variazione del rapporto k4/k5 tra i reattori che si somma al terzo punto;
- variazioni delle alimentazioni in composizione oltre che portata e le maggiori Temperature rispetto a CSTR1à effetti più significativi nei reattori CSTR2 e PFR.
ANDAMENTO DEL PESO MOLECOLARE MEDIO
 |
| ANDAMENTO PESO MOLECOLARE MEDIO NUMERICO |
 |
| ANDAMENTO PESO MOLECOLARE MEDIO PONDERALE |
L’andamento del peso molecolare medio ponderale
è identico a quello numerico ma spostato a valori più alti secondo l’indice di
polidispersità; ciò è dovuto al fatto che tiene più conto delle catene a
maggiore peso molecolare, così come le frazioni massiche tengono più conto
delle sostanze a maggior peso molare rispetto alle frazioni molari: ad esempio,
se abbiamo 10 cubi metallici e 10 di
legno di uguali dimensioni, possiamo decidere di calcolare la frazione di
metallo scegliendo come unità il cubo/volume oppure la massa dei cubi; nel primo caso
la frazione di metallo sarà 10/20 =0.5 cubi di metallo/cubi totali; nel secondo
caso sarà:
il quale è apparentemente maggiore del precedente
valore come anche:
LA
FORMA È DIVERSA MA SI RIFERISCONO ALLO STESSO ASPETTO FISICO/LO STESSO
POLIMERO, ANALIZZANDOLO DA PUNTI DI VISTA DIFFERENTI E DANDOCI INFORMAZIONI
DIFFERENTI.
Tutti e due risultati ci fanno capire quanto
sono distribuiti i pesi molecolari: ad esempio il rapporto delle frazioni di
metallo è circa due e ciò indica che molti cubi hanno massa(MW) minore in
quanto se tutti i cubi avessero stessa massa di quello in metallo (cioè omopolimeri
di uguale lunghezza), tale rapporto sarebbe unitario:
Il rapporto
è detto indice di polidispersità e ci indica quanto è “stretta” la
distribuzione dei MW.
Se vale 1 il polimero è monodisperso, all’aumentare di
tale valore aumenta la dispersione.
L’andamento di tale indice al variare della portata è il seguente:
Gli indici variano di poco. Nel primo reattore crescendo di meno le catene al diminuire del tempo di
permanenza(aumento di portata) e avendo conversione minore e meno catene, quelle
reazioni legate dalla legge cinetica alla concentrazione del polimero radicalico, che già
si è detto avvenire in modo più pesante negli altri reattori, diminuiscono
ancor di più il loro peso cosicché essenzialmente si veda che via via che diminuisce il tempo di permanenza, le
molecole tendono a propagarsi subendo minori interruzioni (anche se si tenga conto che i radicali non si formano tutti
istantaneamente allo stesso momento); risultato IPD diminuisce all’aumentare
della portata per il polimero in OUTCSTR1.
L’andamento dell’IPD del polimero nelle correnti uscenti dagli altri
reattori è opposto. Si noti che mentre il primo non subisce variazioni della
composizione della corrente in ingresso in funzione della portata gli altri
vedranno una corrente che invece cambia anche di composizione. In effetti se per il primo reattore l’effetto
osservabile è identico a quello che si osserverebbe diminuendo il volume del
reattore, per gli altri non è così in quanto oltre al tempo di permanenza cambia
l’alimentazione. L’alimentazione risulta più ricca di stirene all’aumentare
della portata; essendo le cinetiche favorite dall’aumento di temperatura si
osserva in CSTR2 il solito salto di conversione; si noti che le differenze di
conversione tra CSTR2-CSTR1 e PFR-CSTR2 si mantengono all’incirca costanti; sebbene vi sia la diminuzione del tempo di permanenza vi è anche un aumento della frazione di monomero in ingresso cioè una maggiore
velocità di propagazione.
In effetti le curve di conversione risultano praticamente parallele ed
aventi il medesimo andamento della conversione CSTR1; questo vale finché si
considera la conversione rispetto al feed, intrinsecamente la conversione
diminuisce, perché si tiene in conto che ne arriva di più rispetto a prima.
Questo salto di conversione avviene in presenza di più radicali polimerici, più TBP e stirene
in funzione dell’aumento di portata o diminuzione di conversione.
La minore conversione in CSTR1 porta ad una minore presenza di polimero al
massimo MWmedio come visto in precedenza e quindi ad una maggiore influenza di
ciò che succede nei reattori successivi, il quale tende ad abbassare il
MWmedio.
Essendo IPD il rapporto tra MWw e MWn vediamo quale dei due influenza
l’innalzamento dell’IDP; siccome entrambi diminuiscono l’unica possibilità è
che il MWw diminuisca meno del MWn.
Ciò significa che dal punto di vista numerico vi saranno più molecole a MW
basso rispetto al caso di portate inferiori; d’altro canto pesando meno, queste
ultime influenzano in via minore il MWw.
Alla fine si conclude che quando la portata aumenta la polimerizzazione
procede maggiormente negli altri due reattori dove le cinetiche, anche quelle
di trasferimento, sono superiori: il risultato finale è una crescita maggiore delle
macromolecole a peso molecolare relativamente basso, in relazione ai casi a
portata inferiore.
Stessa cosa avviene nel PFR dove le relazioni si sviluppano puntualmente
lungo la lunghezza in modo costante rispetto al tempo e non nell’intero volume
del reattore.
Si noti un particolare: se nel CSTR2 possiamo dire che avvengono
maggiormente le reazioni di trasferimento e terminazione/inizio perché in uscita, cioè
nel reattore, vi è una maggiore percentuale di radicali polimerici, in PFR dobbiamo dire
che queste avvengono sostenute perché prendono la corrente in uscita da CSTR2
che subisce una ulteriore conversione lungo la lunghezza del PFR, essendo la
reazione sviluppata lungo il condotto.
Imponendo la temperatura in uscita del terzo reattore tra 160 e 240°C si
avrà una variazione solo della corrente in uscita del PFR a parità di portata
(quella del caso base).Per una temperatura in uscita pari a 160°C si lavora isotermicamente, mentre per temperature superiori si ha un profilo sempre più pronunciato.
Ovviamente se la temperatura aumenta, lo faranno anche le cinetiche e
quindi la conversione. Non si ha un aumento esponenziale perché all’aumento
delle cinetiche è correlato anche il consumo più rapido di monomero, ciò è osservabile
nel seguente grafico:
Per quanto riguarda invece i MWmedi, l’aumento di conversione in presenza
di una più alta concentrazione di radicali polimerici corrisponde a maggiori catene corte
formate per la grande influenza delle reazioni di trasferimento e terminazione
favorite inoltre dall’aumentare della temperatura.
Si convertiranno più monomeri ma questi formeranno polimeri a catena più
corta che abbasseranno in modo sensibile il MWmedio. In effetti in
corrispondenza di cinetiche superiori si hanno consumi maggiori di monomero che
rallentano la propagazione e favoriscono le altre reazioni di trasferimento e
terminazione. Le due giocano come più volte ribadito.
Allo stesso modo di prima le catene più piccole formate influenzano in modo
diverso i MWmedi; quello numerico subirà un abbassamento relativo maggiore di
quello ponderale; più le catene formate saranno piccole maggiore sarà il
discostamento dei due MWmedi.
In effetti è possibile vedere come l’indice di polidispersità aumenti in
modo più che lineare con la Tout del PFR.
I 200°C sono all’inizio della fase di aumento molto pronunciato; questa
temperatura scelta per il caso base potrebbe essere il risultato di questo tipo
di analisi legata alle proprietà applicative del materiale.
Modificando la frazione massica di iniziatore nell’alimentazione si vuole
studiare l’andamento dei parametri presentati, monitorati al variare della
portata. Non è possibile ovviamente effettuare una sensitività controllando una
frazione massica perché al variare di questa varierebbero:
- le restanti
frazioni secondo una legge ignota ad Aspen;
- la portata
anche se di poco.
Aspen per questo non ha tra le variabili controllate le frazioni dei
componenti in miscela.
Si premette che si potrebbe comunque variare la portata parziale di TBP e
le altri grandezze non subirebbero molte variazioni poiché si tratta di una
frazione piccola dell’alimentazione.
A livello rigoroso si preferisce fare in modo differente.
Si presenta adesso il flowsheet che verrà commentato in seguito.
Si è sdoppiata l’alimentazione in:
- FEED TBP che sarà quella contenente solo TBP, la
quale varierà di portata tra 7000*0.0003 kg/hr e 7000*0.003 kg/hr (cioè portata
base per il range di frazioni analizzate);
- FEED1 che invece è quella che contiene gli altri
componenti in frazione su base priva di TBP, cioè:

Per simulare la variazione di frazione massica cosa si fa?
- Si fa una design-specification dove si impone
che la portata massica di FEED (corrente di mixing tra FEED1 e FEEDTBP) sia
pari a 7000kg/hr variando FEED1.
- Si mantiene attiva la DS.
- Si fa partire una sensitività che monitora i
parametri richiesti facendo variare FEEDTBP tra i valori estremali.
L’obiettivo è quello di variare la frazione di TBP mantenendo in
proporzioni relativamente costanti le altre frazioni, abbassandone solo la
portata totale.
Durante ogni calcolo sulla sensitività verrà generato un loop in Aspen
(simile ad un loop di controllo sulla portata) che ad ogni variazione di
portata di TBP fa corrispondere una variazione complementare a 7000kg/hr di
FEED1.
Il funzionamento del sistema può essere verificato nel pannello di
controllo, un loop compare ad ogni giro di sensitività prima del calcolo su
CSTR1-2 e PFR; inoltre varia (di poco) la portata (monitorata) di stirene in
FEED, cosa che non avverrebbe se ad ogni giro di sensitività non intervenisse
la DS.
Nota la portata di Styrene in FEED1 e dividendo per la sua frazione si può
verificare la complementarità a 7000kg/hr delle due correnti:

A partire dalle portate di FEEDTBP si può facilmente risalire alle frazioni
in peso dividendo per 7000 (uguali unità di misura).
Risolto questo problema, si procede adesso con l’analisi dei risultati.
Ci si aspetta, avendo aumentato la quantità di iniziatore, una maggiore
formazione di catene e quindi un corrispondente aumento della conversione ed
abbassamento del MWmedio(dipendenza inversa del grado di polimerizzazione con [In]0.5); si
formeranno catene più numerose ma più piccole. Si può notare come in ogni caso
l’iniziatore sia convertito totalmente alla fine del processo e quindi quanto
detto è più che valido.
Si potrebbe pensare che aumentando l’iniziatore si formino catene che
comunque possono crescere quanto prima, ciò è valido se non si considerano:
- reazioni di trasferimento e terminazione;
- esaurimento del monomero ergo limite della
conversione che già nel primo caso è 0.83 in uscita.
Quindi il secondo pensiero è sbagliato.
La maggiore conversione è dovuta al fatto che la reazione di inizio è
più sostenuta come anche quella di propagazione vedendo più radicali, laddove
il monomero è in eccesso.
La velocità di propagazione aumenta perché ci
sono più radicali non perché ci sia più monomero e quest'ultimo tenderà a diminuire più
velocemente proprio perché vi sono tante catene che si propagano; bisogna tener
conto delle altre reazioni che riducono il MWmedio che sono ancora più pesanti
perché un numero più grande di catene è presente. Alle alte conversioni le curve (conversione vs TBP) si appiattiscono perché
le cinetiche sono rallentate dalle basse concentrazioni di stirene; se
immaginassimo la conversione costante, aumentando il numero di catene formate
diminuirebbe forzatamente il MWmedio (si può vedere in maniera molto, forse
anche troppo, semplicistica come nella nucleazione di sali in
sovrasaturazione).
Quindi essenzialmente nel CSTR1 le catene saranno più numerose e più
piccole all’aumentare della frazione di iniziatore; gli altri reattori avranno
una alimentazione influenzata da quanto detto: maggiori catene e minore
monomero significa abbassamento maggiore di MWmedio; si noti infatti un
andamento molto simile per CSTR1 e CSTR2, mentre l’andamento della conversione
è smorzato per PFR laddove è la concentrazione di monomero limitante (alte
conversioni): all’aumentare della frazione di TBP intrinsecamente la
conversione nel PFR diminuisce proprio per quanto detto.
Visto che l’abbassamento di MWmedio nel secondo e terzo reattore è dovuto a
maggiori trasferimenti e terminazioni/inizi, in presenza di catene più numerose,
anche l’utilizzo di agenti di trasferimento aumenta. Ad esempio per EB si ha un
aumento in pratica lineare con l’aumento di TBP:
Andamento simile si ha per il secondo agente di trasferimento.
Di seguito vengono riportati dati ed andamenti dei MWmedi numerici e
ponderali:
All’aumentare dell’iniziatore si può benissimo
vedere che l’essenziale della conversione avviene in CSTR1-2: ciò non va tanto
d’accordo con quanto detto all’inizio sulla necessità di utilizzare un PFR ed
in pratica non è realistico. Per questo le modifiche che avvengono in PFR
in termini MWmedio sono in pratica nulle laddove le conversioni sono molto alte,
anche per la maggior prevalenza dell’accoppiamento delle catene che compensa le altre reazioni che tenderebbero a diminuire il
MWmedio.
Se si vuole precisare, la qual cosa è abbastanza inutile, si ha un
piccolo e insensibile aumento del MWmedio in OUTPFR ripetto a OUTCSTR2 spiegabile
sempre con quanto detto, laddove l’accoppiamento delle catene ormai quasi
totalmente formate superi come effetto l’insieme delle altre reazioni.
Quest’ultimo effetto è ancora più visibile nel MWmedio ponderale visto che
l’accoppiamento porta da due catene radicaliche ad una più grande non
radicalica: nel MWn la catena aumenta ma diminuisce il numero di tali catene,
nel MWw si tiene più in conto l’aumento della massa della catena più pesante.
L’indice di polidispersità assume un andamento particolare:
Per CSTR1 si ha l’andamento monotono decrescente; all’aumentare della
frazione di iniziatore si ha un maggior numero di inizi, catene formate
più piccole ma più omogenee come distribuzione,
lavorando in grandi quantità di monomero; ciò rappresenta il fatto che
all’aumentare degli inizi è il numero di catene che fa la differenza, la
velocità di propagazione aumenta per queste, mentre il contributo alle catene dei
monomeri è più piccolo proprio perché vi sono più catene e meno monomero per
catena del caso base: più catene che si possono propagare di meno: il MWw ha la
possibilità di spostarsi meno dal MWn. Lavorando il reattore tutto in medesime
condizioni ne risulta maggiore omogeneità del polimero.
Negli altri reattori invece l’andamento non è monotono ma si ha un minimo.
Inizialmente l’aggiunta di iniziatore diminuisce l’IDP mentre sale dopo un
valore di frazione massica di TBP nel feed compreso tra 0.0015 e 0.0018 per
CSTR2.
Cosa cambia per CSTR2 variando la frazione di TBP?
Varia l’alimentazione che ha MWmedio più piccolo e meno distribuito e la
quantità di TBP stesso che arriva che è maggiore, all’aumentare della sua
frazione.
Cosa indica questo andamento?
Che inizialmente il MWw scende più rapidamente del MWn e invece
successivamente il MWw scende meno rapidamente del MWn.
L’andamento nel terzo reattore è strettamente legato a quello nel secondo
dove si ha “il grosso” della conversione.
L’indice di polidispersità dipende da come ed in che condizioni concorrono trasferimento e inizio/accoppiamento.
Inizialmente come nel CSTR1 l’aumento della quantità di iniziatore fa in
modo che si abbiano catene più piccole e più omogenee; quando si raggiungono
livelli di conversione molto elevati per CSTR2 si ha che si formano molte
catene più piccole rispetto alla media ponderale che finiscono per far risalire
l’indice di polidispersità. In pratica in un certo istante la concentrazione di
monomero è così bassa da poter avere che quando i radicali si formano, dopo una crescita molto più limitata, si
accoppiano sviluppando catene più corte tra formazione ed accoppiamento.
Ciò porta ad una riduzione più repentina del MWn e quindi l’innalzamento
del IPD. Nota: l’iniziatore si esaurisce in PFR in ogni caso.
L’andamento in PFR è l’effetto di ciò che avviene in CSTR2; siccome si
lavora a conversioni maggiori l’andamento tende ad essere più propenso “alla
risalita” ma effettivamente è ciò che succede in CSTR2 a prevalere.